Livre étudiant – Dihydrogène
Partie 1 : Production et consommation du dihydrogène
Contrairement au pétrole, au charbon ou au gaz naturel, quasiment aucun gisement de dihydrogène, déjà présent en l’état, n’a été découvert sur notre planète. (cf l’espoir suscité par la découverte récente d’un gisement potentiel de dihydrogène en Lorraine).
A ce jour, il doit donc être produit en utilisant de l’énergie pour séparer le dihydrogène d’une molécule qui en contient : de l’eau (H2O) ou du méthane (CH4) par exemple.
Le vaporeformage est une technique de production du qui permet non seulement de récupérer l’hydrogène du méthane par réaction (endothermique) avec de la vapeur d’eau sur un catalyseur au nickel. Cette transformation a lieu à haute température (840 à 920°C), à pression modérée (de l’ordre de 20 à 30 bars) et aboutit ainsi à un gaz de synthèse riche en H2. L’hydrogène pur est obtenu ensuite par séparation d’avec le CO2 par un procédé membranaire. (Réaction chimique global : CH4 + 2H2O ↔ CO2 + 4H2).
L’oxydation partielle peut être effectuée sur des produits plus ou moins lourds. A haute température (classiquement de 900 à 1500 °C) et à pression élevée (classiquement 20 à 60 bars), en présence d’oxygène en tant qu’oxydant et d’un modérateur de température (la vapeur d’eau), l’oxydation partielle des hydrocarbures conduit également à la production de gaz de synthèse. En revanche, la réaction est exothermique et se déroule (en général) sans catalyseur. (Réaction chimique global : CnHm + nH2O + (n/2)O2 ↔ nCO2 + (n+m/2)H2).
L’électrolyse permet de décomposer chimiquement l’eau en dioxygène et dihydrogène sous l’action d’un courant électrique. Actuellement, la production de dihydrogène par électrolyse coûte 3 à 4 fois plus cher que la production par reformage du gaz naturel et souffre de plus d’un mauvais rendement global, cependant celle-ci n’est pas émettrice de GES.
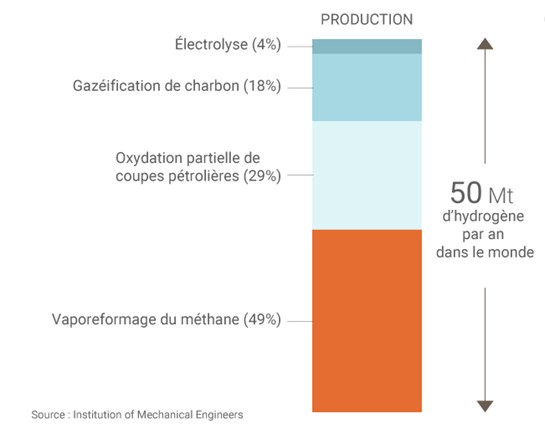
Production du dihydrogène dans le monde en 2015, dans "France: 100 millions d'euros pour le plan hydrogène" Connaissance Des Energies, 2018.
[Utilisé avec l'autorisation de Connaissance Des Energies]
Les appellations de couleur du dihydrogène sont déterminées en fonction du type d’énergie employé dans le processus de production et de son origine, renouvelable ou non. Comme vu précédemment, il y a plusieurs façons de produire de l’hydrogène : à base de charbon, de gaz naturel (méthane) ou encore d’eau. Chaque méthode de production est associée à une couleur selon son impact environnemental. S’il est produit à partir de charbon, il est très polluant donc la couleur associée est très foncée. S’il est produit à base de gaz naturel, on le qualifie de « gris » car il est également émetteur de gaz à effet de serre, mais il peut être bleu si le dioxyde de carbone émis lors de sa production est stocké et réutilisé. L’hydrogène peut être aussi produit grâce à l’électrolyse de l’eau. Enfin, selon si l’électricité utilisée pour alimenter l’électrolyseur provient du nucléaire, ou est d’origine solaire, éolienne ou hydroélectrique, la couleur associée sera différente. Mais bien entendu, d’un point de vue scientifique, le gaz dihydrogène n’a pas réellement de couleur.
2. Compléter le tableau ci-dessous, en utilisant les listes suivantes :
- Procédés : gazéification / électrolyse / vaporeformage
- Matières premières : méthane / eau / charbon / dihydrogène
- Énergie : Énergie renouvelable / Combustibles fossiles / Énergie nucléaire
| Couleur | Procédé | Matières premières | Énergie |
| Noir | |||
| Gris | |||
| Bleu | |||
| Rose | |||
| Jaune | |||
| Vert | |||
| Blanc |
3. Commenter les principaux usages du dihydrogène.
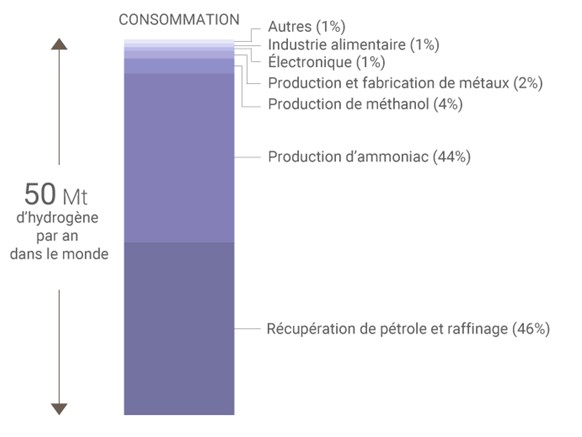
[Utilisé avec l'autorisation de Connaissance Des Energies]
Le coût de production et l’empreinte carbone de l’hydrogène dépendent fortement de son mode de production comme présenté dans le tableau ci-dessous.
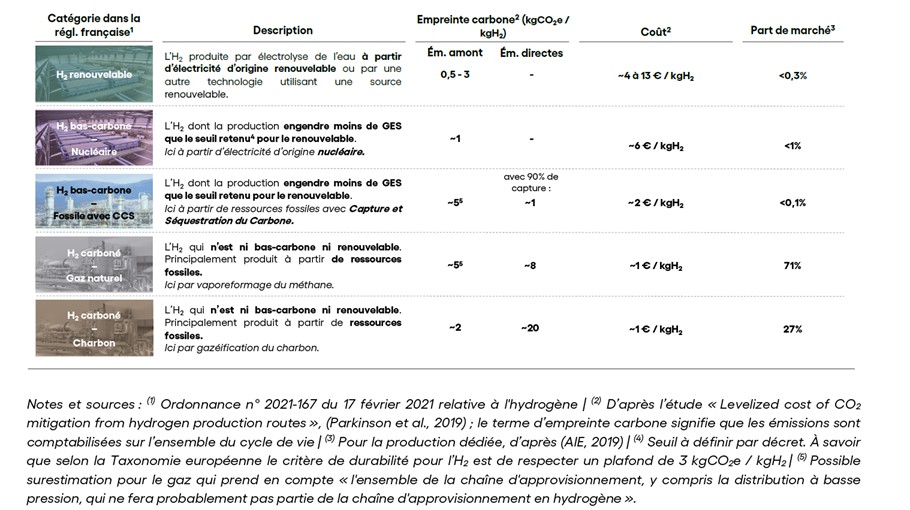
Source : Hydrogène bas-carbone : quels usages pertinents à moyen terme dans un monde décarboné ? Etude Carbone 4 – Octobre 2022 (GES : Gaz à effet de serre / CCS : Carbone Captur Storage : Em : Emissions)
[Utilisé avec l'autorisation de Carbon 4]
4. A partir des données présentées dans le tableau ci-dessus et en réalisant une moyenne pondérée sur les parts de marché, calculer l’empreinte carbone actuelle (exprimée en kgCO2e/kgH2) du dihydrogène.
Pour décarboner la production actuelle de dihydrogène, le procédé d’électrolyse de l’eau suscite beaucoup d’espoir.
L’électrolyse de l’eau s’effectue, selon la réaction suivante à partir d’électrodes inertes électrochimiquement, réalisée en conditions basiques (pH=14) et à température ambiante :
H2O(l) → H2(g)+ 1/2 O2(g) (réaction 1)
5. Développer un raisonnement thermodynamique pour justifier que cette réaction n’est pas spontanée et nécessite pour se faire, l’apport d’un travail électrique.
6. Représenter schématiquement le dispositif d’électrolyse correspondant à cette réaction. Préciser le sens du courant, ainsi que la nature de chaque électrode (cathode, anode) et les réactions qui s’y produisent.
7. Donner les expressions littérales des équations de Nernst pour les deux couples redox en considérant l’électrolyse de l’eau réalisée en conditions basiques.
8. En déduire l’expression littérale de la différence de potentiel entre les deux électrodes.
9. Calculer la tension minimale à appliquer aux électrodes pour que la réaction d’électrolyse soit possible. Nous considérerons que les gaz sont tous les deux à la pression standard.
On souhaite produire 1,00 kg de dihydrogène à p=1,00 bar et T=298 K.
10. Calculer la masse d’eau nécessaire pour cette production.
11. Calculer la quantité d’énergie électrique (en kWh) nécessaire. Discuter les limites de ce calcul en analysant la Figure 1 en données.
12. Sachant que le dihydrogène est qualifié de « H2 bas-carbone » si et seulement si son empreinte carbone est inférieure ou égale à 3 kgCO2e / kgH2, dans quel-s pays la production de dihydrogène par électrolyse de l’eau permettrait de respecter ce critère ? Vous utiliserez pour répondre à cette question les données de la Figure 2 en données.
