Livre étudiant – Dihydrogène
Partie 2 : Recours au dihydrogène
Le domaine de la mobilité
L’un des verrous pour l’utilisation du dihydrogène en tant que vecteur d’énergie dans le domaine de la mobilité est son stockage. Il doit permettre d’avoir d’une part, un haut degré de sécurité et d’autre part, des facilités d’usage (capacités de stockage – dynamique de stockage/déstockage) pour permettre de fonctionner dans des conditions techniques acceptables. Pour que le dihydrogène devienne une solution viable, les procédés de stockage devront donc être sûrs, économiques et adaptés à une multitude d’utilisations dans le futur : applications mobiles pour le transport et dispositifs portables ou stationnaires.
Les constructeurs automobiles, par exemple, demandent une autonomie de 500 km environ ; compte-tenu du pouvoir calorifique du dihydrogène il est nécessaire d'en stocker 5 kg. Dans cette partie, nous allons tenter de comparer différentes formes de stockage.
Le stockage du dihydrogène gazeux sous forme comprimée est le moyen de stockage le plus utilisé actuellement et se fait sous une pression de 350 bar à une température de 298 K dans un réservoir composite.
a.Calculer le volume de réservoir nécessaire aux 500 km d’autonomie en considérant qu’il est égal au volume occupé par le dihydrogène gazeux.
b.On suppose qu’un réservoir vide d’1 m3 a une masse de 400 kg. Calculer la masse du réservoir vide susceptible de contenir le volume de dihydrogène gazeux calculé à la question précédente.
c.Calculer la capacité de stockage sous cette forme (en kg.m-3)
d.Calculer le pourcentage massique de H2 dans cette forme.
Le stockage sous forme liquide se fait à une température de 20 K (-253 °C) sous une pression de 1,0 bar. Dans ces conditions, la masse volumique du dihydrogène liquide est
(ρH2(l)) = 70,8 kg.m-3.
a.Calculer le volume de réservoir nécessaire aux 500 km d’autonomie en considérant qu’il est égal au volume occupé par le dihydrogène liquide.
b.On suppose toujours qu’un réservoir vide d’1 m3 a une masse de 400 kg. Calculer la masse du réservoir vide susceptible de contenir le volume de dihydrogène liquide calculé à la question précédente.
c. Calculer la capacité de stockage sous cette forme (en kg.m-3)
d.Calculer le pourcentage massique de H2 dans cette forme.
On peut aussi envisager de stocker le dihydrogène à l’état condensé sous forme d’hydrure par chimisorption. Le dihydrogène est alors absorbé par un substrat comme l’alliage FeTi. Cet alliage a une maille cubique simple avec un atome de titane à chaque sommet du cube et un atome de fer au centre du cube (Masse molaire Fe : 55,845 g.mol-1 et masse molaire Ti : 47,867 g.mol-1) (fiche N°221 en données).
a.Représenter la maille et définir de quelle structure type il s’agit ?
b.Définir le mode de réseau, le système cristallin, le réseau de Bravais et le groupe d’espace de cette maille.
c.Déterminer la coordinence du Fe vis-à-vis du Titane et inversement.
d.Sachant que le paramètre de maille vaut 2,975 Å. Calculer la masse volumique de ce composé.
e.Caractériser le nombre et les positions des sites interstitiels. Sont-ils réguliers ? Justifier.
f.Les sites octaédriques seront-ils déformés après introduction d’un atome d’hydrogène ? Justifier.
(rFe = 1,25Å , rTi = 1,45 Å, rH = 0,350 Å)
L’absorption du dihydrogène par l’alliage FeTi se fait selon la réaction suivante : FeTi(s) + n/2 H2(g) → FeTiHn(s).Dans ce composé FeTi, les hydrogènes viennent se loger dans les sites interstitiels de type octaédrique.
g.Représenter la maille de l’hydrure formé à l’issu de la réaction si tous les sites susceptibles d'accueillir des atomes d'hydrogène sont occupés.
h.En déduire la formule stœchiométrique de l'hydrure contenant le maximum possible d’hydrogène.
i.Donner les positions de Wyckoff (site cristallographique) des différents atomes. Vérifier la cohérence avec la réponse précédente.
En réalité la formule de l’hydrure est FeTiH1,9. Et pour la suite de l’exercice nous allons faire que la maille reste cubique.
j. Quelle masse d’alliage doit-on utiliser pour stocker les 5 kg de dihydrogène nécessaires aux 500 km d’autonomie ?
k.Calculer le volume de réservoir nécessaire aux 500 km d’autonomie.
l. Calculer la capacité de stockage de cette méthode.
m.Calculer le pourcentage massique de H2 dans ce système de stockage en considérant que le réservoir à une masse de 15 kg.
| État physique | Volume stockage (L) |
Pression (bar) |
Température (°C) |
Capacité de stockage (kg.m-3) |
% masse H2/système |
| Stockage gazeux | |||||
| Stockage liquide | |||||
| Stockage solide |
| Stockage gazeux | Stockage liquide | Stockage solide | |
| Avantages | |||
| Inconvénients |
Intéressons-nous à présent plus précisément au cas d’un camion à hydrogène à propulsion électrique doté d'une pile à combustible utilisant du dihydrogène comme combustible. Hyundai propose un modèle de 18 tonnes opérationnel depuis Mars 2020, le Hyundai XCient. Celui-ci est équipé d'une pile à combustible et de réservoirs haute pression contenant 32 kg de dihydrogène. L'autonomie annoncée de ce camion Hyundai est de plus de 400 kms.
Selon les calculs de l’Atelier d’écologie politique, afin de remplir les objectifs européens pour 2030 et alimenter en hydrogène vert ne serait-ce que 100 000 camions de plus de 16 tonnes parcourant une moyenne de 160 000 km/an, il faudrait l’équivalent de 15 réacteurs nucléaires.
Source : Greenwashing, Manuel pour dépolluer le débat public – éditions du Seuil, sous la direction de A.Berlan, G.Carbou et L.Teulières, page 218 (chapitre Véhicule propre)
Pour aller plus loin dans cette réflexion, il est possible de proposer de consulter tout ou partie du rapport Hydrogène bas-carbone : quels usages pertinents à moyen terme dans un monde décarboné ? Etude Carbone 4 – Octobre 2022.
Données :
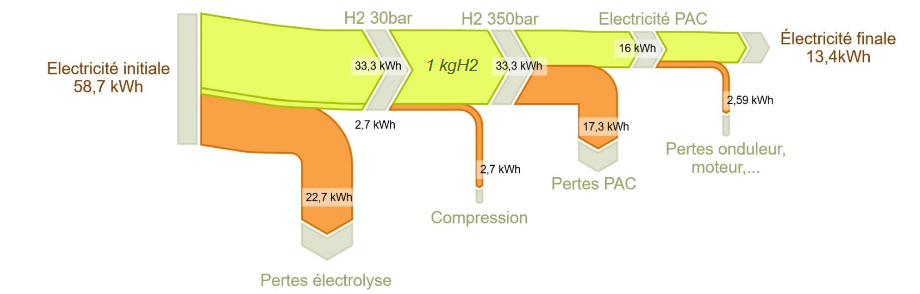
Figure 1 : Diagramme de Sankey exprimant l’énergie nécessaire pour produire un kg de dihydrogène ainsi que l’énergie électrique résultante.
[source : Fiche Technique ADEME Rendement de la chaîne hydrogène, cas du « power-to-H2-to-power », Janvier 2020]
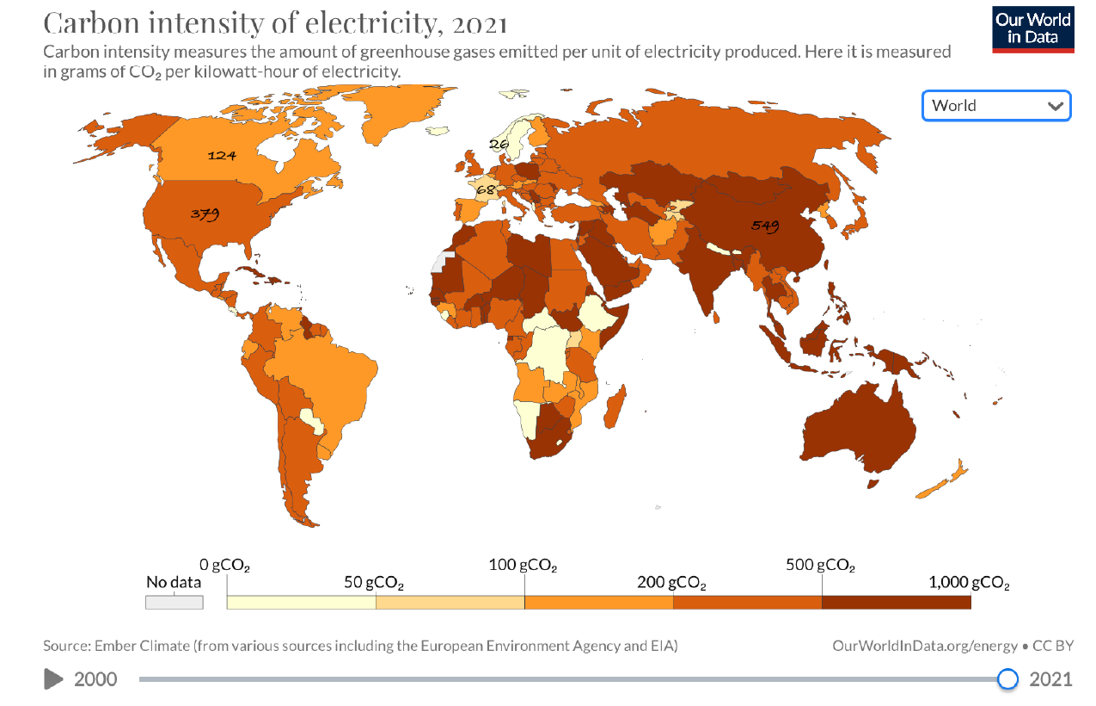
Figure 2 : Intensité carbone de l’électricité à travers le monde en 2021 (exprimée en gCO2e/kWh)
[source : Our World in Data]
Potentiels standard à pH = 14
½ O2/OH- : E° = + 0,40 V
H2O/H2 : E° = - 0,83 V
Demi-réactions :
½ O2/OH- : 1/2 O2(g) + H2O(l)+2e-→ 2OH-(aq)
H2O/H2 : 2H2O(l) + 2e- → H2(g) + 2OH-(aq)
A (ampère) = C.s-1 ; Constante de Faraday : F = 96 500 C.mol (d’e-)-1
Produit ionique de l’eau Ke = 10-14
Table enthalpies standard de formation et entropies standard pour H2(g), O2(g) et H2O(l) :
| DfH° (kJ.mol-1) | Sm° (J.K-1.mol-1) | |
| H2O | -285,8 | 69,9 |
| O2 | 0 | 205,2 |
| H2 | 0 | 130,7 |
En 2021, le parc nucléaire français, composé de 56 réacteurs à eau pressurisée en service, a produit 360,7 TWh de travail électrique [source].
Sources d’inspiration :
CCINP Chimie MP 2002
TSICH07 EPREUVE SPECIFIQUE - FILIERE TSI 2011
CHAP 04-ACT PB/DOC Electrolyse de l’eau
Bac S Antilles Spécialité 2014
Ressources pédagogiques discipline Chimie – INSA Lyon
